Forsøg 1.2 - Ethanols kogepunkt:
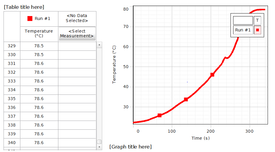
Vi har en bunsenbrænder og en stativ, som vi sætter et reagensglas og termometer fast på. Vi har et bægerglas hvor vi hælder vand i, da reagensglasset skal være i et vandbad. I reagensglasset er der 1-2 centimeter sprit/ethanol. Vi tænder bunsenbrænderen og skal finde ud af hvor mange grader dampen fra spritten skal være, for at det koger. Vi kan konkludere at ethanol koger ved 78,6 grader, det gør det efter 5 minutter og 39 sekunder. Termometeret skal være 1-1½ centimeter fra væsken/spritten, da det er dampen vi skal tage, og derfor må termometeret heller ikke røre ved reagensglassets sider.
På billederne kan man se, hvordan vi har opstillet forsøget, og hvordan de forskellige væsker udvikler sig i løbet af processen. På det nederste billede til højre er der vist en graf, som viser stigningen på graderne.
Alkohol i hverdagen:
Alkohol er det dagligdagens ord for stoffet ethanol. Efter indtagelse af meget alkohol, oplever man en rus, og man siges at være fuld eller beruset. Efter rusen får man hovedpine, svimmelhed, kvalme samt generel ubehag af vekslende styrke, som kaldes tømmermænd. Ved længerevarende overforbrug af alkohol kan der opstå skader på kroppens organer og/eller alkoholafhængighed.
Der er alkohol i nogle rengørings midler, håndsprit, neglelakfjerner og hår produkter.
Bio alkohol kommer fra majs planter - den slags alkohol der kommer fra neglelakfjerner.
Der er alkohol i nogle rengørings midler, håndsprit, neglelakfjerner og hår produkter.
Bio alkohol kommer fra majs planter - den slags alkohol der kommer fra neglelakfjerner.
Alkoholgæring:
I dette forsøg starter vi med, at veje 25 g. sukker af i en kolbe. Derefter tilsætter vi 200 ml. vand og ryster kolben til sukkeret er helt opløst. Når det er opløst, tilsætter vi 10 g. bagegær og ryster igen kolben, indtil gæren er fint fordelt. Derefter sætter vi en prop med et hul i kolben, og i hullet sætter vi et glasrør, som er forbundet med et andet glasrør via. en slange. Det andet glasrør går over i et reagensglas, som er 1/4 fyldt op med vand. Denne opstillig lader vi stå i 1-2 uger.
6.1 alkoholgæring - destillation
Dette forsøg er opstillet som vist på billederne ovenover. Formålet ved dette forsøg er, at vi skal skille ethanolen fra gæringen, hvilken sker ved en fordampning. Vi starter med at varme gæringsprocessen op, og den skal hele tiden være omkring de 78-88 grader. Det er vigtigt, at temperaturen er jævn, fordi ellers kan glasset sprænge, og så virker forsøget selvfølgelig ikke. For at holde temperaturen jævn, bliver vi nødt til at fjerne bunsenbrænderen frem og tilbage fra kolben. Når vi har gjort det nogle gange, begynder ethanolen langsomt at sive op gennem det lille glasrør, videre ned gennem slangen og til sidst ned i reagensglasset. Som man kan se på billederne, er reagensglasset placeret i et glas med vand, som er nedkølet med isterninger. Det er fordi, at det skal blive til vand og ikke gas. Dette fortsætter vi så bare med nogle gange, og reagensglasset bliver langsomt mere og mere fyldt med ethanol. Det er en meget langsom process, og derfor tager det lang tid bare at opsamle 1 cm. ethanol.
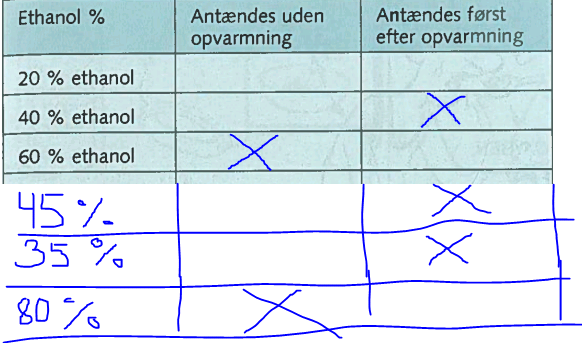
3.1 Antændelse af alkohol
Vi har en teske, hvor vi skiftevis tager 10-15 dråber af forskellige procent ethanol. Man kan se at jo højere procenten er, kan ethanolen lettere brænde, og jo lavere, kan det ikke brænde eller skal opvarmes før det kan brænde.
3.4 Energindhold i Ethanol
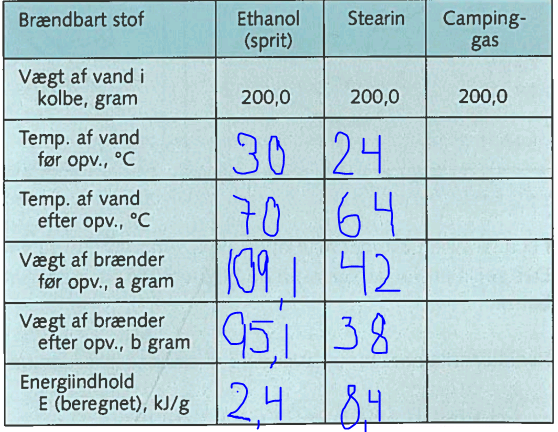
Vi starter med at lave en spritbrænder, og det gør vi ved at putte en tot vat i en porcelænsskål, og hænder noget sprit hen over, så det dækker vattet. Skålen stiller vi på en trefod, og ovenover trefoden har vi sat en kolbe med 200 g vand i fast i et stativ. Meningen er nu, at vi skal få temperaturen på vandet til at stige ved at sætte ild til spritbrænderen. Ifølge forsøget skal temperaturen stige 40 grader, før vi kan slukke spritbrænderen igen. Til sidst beregner vi energiindholdet, som kan se på skemaet nedenunder.
Efter forsøget med spritbrænderen, bytter vi brænderen ud med et stearinlys og gør nøjagtigt det samme som før. Her går det bare meget langsommere, fordi flammen er en del mindre.
Efter dette forsøg kan vi konkludere, at spritbrænderen er bedst tidsmæssigt, men at stearinlyset er bedst energimæssigt, når vi beregner hvor meget sprit, der er i ethanol.
Efter forsøget med spritbrænderen, bytter vi brænderen ud med et stearinlys og gør nøjagtigt det samme som før. Her går det bare meget langsommere, fordi flammen er en del mindre.
Efter dette forsøg kan vi konkludere, at spritbrænderen er bedst tidsmæssigt, men at stearinlyset er bedst energimæssigt, når vi beregner hvor meget sprit, der er i ethanol.
5.1 Ethanol til ethanal
Ethanol = alkohol
Ethanal = tømmermænd
Vi starter med at dryppe 5-10 dråber ren ethanol i et reagensglas. Så ryster vi det lidt rundt, så der kommer alkoholdampe i glasset. Derefter lugter vi til det, og det lugter lidt ligesom ved tandlægen - sprittet. Derefter tager vi en kobber-spiral og kører op og ned af reagensglasset. Derefter skal vi lugte til det igen, og denne gang lugter det meget mere sprittet. Bagefter putter vi 2,5 ml. alon-indikator i glasset og ryster det endnu en gang. Ved at gøre det, skal vi finde ud af, om der kommer bundfald - og det gør der ikke.
Bagefter gentager vi det hele, men inden vi stikker kobbertråden ned i reagensglasset, opvarmer vi den over en bunsenbrænder. Derefter kører vi den igen op og ned af reagensglasset. Derefter tilsætter vi igen 2,5 ml. alon-indikator og omryster. Denne gang blev der dannet bundfald.
2 CH3CH2OH + O2 = 2 CH3CHO + 2H2O
Ethanol + ilt -> kobber -> ethanal + vand
Vi kan nu konkludere, at en varm kobbertråd virker som katalysator, så ethanolen bliver omdannet til ethanal.
Ethanal = tømmermænd
Vi starter med at dryppe 5-10 dråber ren ethanol i et reagensglas. Så ryster vi det lidt rundt, så der kommer alkoholdampe i glasset. Derefter lugter vi til det, og det lugter lidt ligesom ved tandlægen - sprittet. Derefter tager vi en kobber-spiral og kører op og ned af reagensglasset. Derefter skal vi lugte til det igen, og denne gang lugter det meget mere sprittet. Bagefter putter vi 2,5 ml. alon-indikator i glasset og ryster det endnu en gang. Ved at gøre det, skal vi finde ud af, om der kommer bundfald - og det gør der ikke.
Bagefter gentager vi det hele, men inden vi stikker kobbertråden ned i reagensglasset, opvarmer vi den over en bunsenbrænder. Derefter kører vi den igen op og ned af reagensglasset. Derefter tilsætter vi igen 2,5 ml. alon-indikator og omryster. Denne gang blev der dannet bundfald.
2 CH3CH2OH + O2 = 2 CH3CHO + 2H2O
Ethanol + ilt -> kobber -> ethanal + vand
Vi kan nu konkludere, at en varm kobbertråd virker som katalysator, så ethanolen bliver omdannet til ethanal.
-
Ethanol - alkohol
Formlen for alkohol - C2H5OH - OH viser at det er et alkohol.
Molekyler, hvor der indgår carbonatomer, defineres som organiske forbindelser.
Ethanol er en organisk forbindelse
To undtagelser - Carbondioxid og Kuldioxid - CO2
Kulmonooxid og carbonmonooxid - CO
Disse to er uorganiske forbindelser.
Ethanol er: En farveløs væske, kogepunkt på 78 grader, frysepunkt på -117 grader, massefylde på 0,795 g/ml (Undersøg andre alkoholer)
Ethanol og energi
Når ethanol brænder forekommer en fuldstændig forbrænding = ingen forurening.
C2H5OH + 3O2 à 2CO2 + 3H2O (Hvidt cuso4 blev blåt - der bruges en CO2 indikator eller kalkvand)
Vand og kuldioxid kan ikke brænde og er derfor defineret som en fuldstændig forbrænding.
Ånding er også en fuldstændig forbrænding - der dannes vand og kuldioxid - respiration
Det modsatte af respiration er fotosyntese.
Kalkvand - Ca(OH)2
Calciumhydroxid
Kan bruges om indikator for CO2
Når calciumhydroxid reagerer med kuldioxid vil der dannes et hvidt uopløseligt bundfald
Calciumcarbonat - CaCO3
Volumenprocent eller vægtprocent
Volumen = rumfang
Vægt = hvad det vejer
Ethanols massefylde (cirka) = 0,8 g/ml
Hvad vejer 500 ml ethanol? - 400 g.
Hvad vejer 500 ml vand? - 500 g.
En overraskelse 500 ml vand + 500 ml ethanol = /1000 ml.
500 ml vand + 500 ml ethanol = 960 ml.
500 ml vand blandet med 500 ml ethanol giver altså:
- en vægt på 900 g.
- og en volumen på 960 ml.
Vægtprocenten
Hvor mange procent udgør 400 g af 900 g?
400 g = vægt af 500 ethanol
900 g = vægt af vand + ethanol
- vægtprocenten
Volumenprocenten
Hvor mange procent udgør 500 ml af 960 ml?
500 ml = ren alkohol
960 ml = ethanol + vand
- volumenprocenten (vol %)
Gæring og destillation
Ethanol dannes ved en kemisk proces, når glukose (druesukker), C6H12O6 under oxygenfrie forhold er i kontakt med bagegær. Samtidig dannes carbondioxid, der er en gas. Når gærbrød hæver, skyldes det netop carbondioxid, dannet ved gæring af sukker. Reaktionsskemaet ser sådan ud:
C6H12O6 à 2 C2H5OH + 2 CO2
Druesukker - Ethanol - kuldioxid
Gæringsprocessen foregår bedst under en lun temperatur, og når gæret får produceret nok ethanol ca. 12-14% vil gæren dræbe sig selv.
Ved destillationen udnytter vi det, at ethanol og vand har forskellige kogepunkt, og derved kun opvarme så ethanolen fordamper. Derved kan vi producere næsten ren ethanol. Vores destillat nåede en alkoholprocent på ca. 55%. Man vi aldrig kunne producere 100% ren ethanol, der vil altid være lidt vand bundet til alkoholen, derfor er det fineste man kan opnå ca. 96-98% ren ethanol.
Ethanol til ethanal
2 CH3CH2OH + =2 à(Cu) 2 CH3CHO + 2 H2O
Ethanol à ethanol
Cu = katalysator
Ethanal kan påvises med en alon-indikator - aldehyd
Ethanol til ethen
C2H5OH à C2H4 + H2=
Ethanol à ethen
Ethanol kan meget nemt omdannes til kulbrinten ethen (ethylen).
Destillation:
Hæld vand med alkohol(efter gæringsprocessen) i en kolbe. Sæt den på en trefod med ild under. Kolben skal være tæt men et rør skal føre ned i en bæreglas, der står i vand. Ethanol koger ved 78 grader, og det er det vi benytter os af for at destillere. Det er godt hvis væsken ligger på ca. 85 grader. Ethanolen vil fordampe over i bægerglasset, derved sker der en fortætning. I kolben vil det være rent vand der er tilbage.