Madens kemi
Disaccharid = 2 sukkermolekyler - hvidt sukker, almindeligt sukker - C12H22O11 (opbygget af de to mono: glucose og fructose)
Monosaccharid = 1 sukkermolekyle - druesukker, glukose, fruktose- C6H12O5
Saccharid = sukkermolekyle
Monosaccharid = 1 sukkermolekyle - druesukker, glukose, fruktose- C6H12O5
Saccharid = sukkermolekyle
Opvarmning af sukker
Vi starter med at putte 1 teske kartoffelmel i et reagensglas. I de to andre reagensglas putter vi 1 teske sukker og druesukker i. Derefter fylder vi reagensglassene halvt op med vand og rører rundt.
Vi tager derefter et stort bægerglas og fylder det halvt med vand. Herefter stiller vi bægerglasset på en trefod over en bunsenbrænder. Vi tænder så bunsenbrænderen og drypper 5-10 dråber benedictreagens i hvert reagensglas.
Udfra farven på opløsningen i reagensglassene, kan vi se, at der er glukose i druesukkerblandingen. Dette glas' opløsning skifter nemlig farve fra blå til brun, hvilken viser, at der er monosaccharid i.
Vi tager derefter et stort bægerglas og fylder det halvt med vand. Herefter stiller vi bægerglasset på en trefod over en bunsenbrænder. Vi tænder så bunsenbrænderen og drypper 5-10 dråber benedictreagens i hvert reagensglas.
Udfra farven på opløsningen i reagensglassene, kan vi se, at der er glukose i druesukkerblandingen. Dette glas' opløsning skifter nemlig farve fra blå til brun, hvilken viser, at der er monosaccharid i.
7.1 spaltning af sukker
I dette forsøg skal vi finde ud af, hvor meget glukose/monosaccharid, vi kan omdanne i en sukkeropløsning.
Vi starter med at opløse 0,95g sukker i et bægerglas. Herefter hælder vi 10 ml fortyndet eddikesyre i sukkeropløsningen. Så opvarmer vi blandingen i 5 minutter. Herefter skal vi neutralisere blandingen. Derfor lader vi blandingen stå og afkøle lidt, inden vi drypper en dråbe af blandingen på et stykke indikatorpapir. Farven er rød, og derfor ikke neutral. Derfor drypper vi lidt ammoniakvand i blandingen, og måler ph'en på et stykke indikatorpapir. Dette fortsætter vi med, indtil indikatorpapiret bliver grønt og neutralt.
Herefter hælder vi blandingen over i et måleglas, og fylder resten af glasset med vand op til 100 ml. Så hælder vi hele blandingen tilbage i bægerglasset og hælder 4 pipetter bendictreagens i blandingen. Derefter varmer vi igen blandingen op, indtil farven skifter fra blå til brun.
Vi kan nu konkludere, at vi har omdannet disaccharid til monosaccharid.
Sukker/glukose i forskellige madvarer:
Abrikossaft: Lidt kraftigt farveskift til mørkere abrikosgul
Cherioes: Ikke så kraftigt farveskift - lysegul
Riskiks: Ikke så kraftigt farveskift - lysegul
Vandmelon: 8,6 g - "karftigt" farveskift til mørkegul
Vi starter med at opløse 0,95g sukker i et bægerglas. Herefter hælder vi 10 ml fortyndet eddikesyre i sukkeropløsningen. Så opvarmer vi blandingen i 5 minutter. Herefter skal vi neutralisere blandingen. Derfor lader vi blandingen stå og afkøle lidt, inden vi drypper en dråbe af blandingen på et stykke indikatorpapir. Farven er rød, og derfor ikke neutral. Derfor drypper vi lidt ammoniakvand i blandingen, og måler ph'en på et stykke indikatorpapir. Dette fortsætter vi med, indtil indikatorpapiret bliver grønt og neutralt.
Herefter hælder vi blandingen over i et måleglas, og fylder resten af glasset med vand op til 100 ml. Så hælder vi hele blandingen tilbage i bægerglasset og hælder 4 pipetter bendictreagens i blandingen. Derefter varmer vi igen blandingen op, indtil farven skifter fra blå til brun.
Vi kan nu konkludere, at vi har omdannet disaccharid til monosaccharid.
Sukker/glukose i forskellige madvarer:
Abrikossaft: Lidt kraftigt farveskift til mørkere abrikosgul
Cherioes: Ikke så kraftigt farveskift - lysegul
Riskiks: Ikke så kraftigt farveskift - lysegul
Vandmelon: 8,6 g - "karftigt" farveskift til mørkegul
7.2 kartOfler (1) + (2)
Vi starter med at skrabe og hakke to kartofler i bitte små stykker (atomer.) Herefter pakker vi kartoffelstykkerne ind i et viskestykke og folder det som en pose, så dypper vi posen i et 500 ml bægerglas, der er halvt fyldet med vand. Derefter presser vi viskestykket, så vandet fra kartoflerne løber ned i glasset. Dette gør vi nogle gange. Bagefter lader vi glasset stå i lidt tid, til der er dannet bundfald. Dette bundfald, vi får dannet, er nøjagtigt det samme som kartoffelmel. Derfor kan vi tilsætte mere kartoffelmel for at fået bedre resultat.
Herefter opvarmer vi 50 ml vand til det koger. Når vandet så koger, tilsætter vi bundfaldet (stivelsen), og rører rundt. Så slukker vi for gassen, og holder bunden af det lille bægerglas (det med stivelsesblandingen) ned i et større glas med koldt vand. Her måler vi temperaturen, indtil den er faldet til 40 grader. Vi har nu fremstillet en stivelses-opløsning.
I næste forsøg fordeler vi en spytblandingen, der består af spyt og vand, i 4 reagensglas. Herefter tilsætter vi 1 dråbe stivelsesreagens i hvert glas. Så tilsætter vi 10 ml af stivelsesopløsningen i det første reagensglas. Derefter tilsætter vi 10 ml i det andet glas, så det tredje og til sidst det fjerde glas. Vi rører rundt i hvert glas efter tilsætningen.
Da alle fire glas har fået tilsat, hvad der skulle, sammenligner vi udseendet på væskerne. Alle væsker er blå, men vi kan se, at jo mere spyt, der er i glasset, jo lysere bliver farven. Det vil sige, at spyt nedbryder stivelsen.
Ved dette forsøg har vi også fundet ud af, at man kan dryppe nogle dråber stivelsesreagens på forskellige madvarer, og så kan man se, at jo mørkere madvaren bliver, jo mere stivelses er der i.
Forsøg 4: Påvisning er stivelse:
- faste stoffer drypper vi en dråbe stivelsesreagens på, for at se om der er stivelse i.
Abrikoser: Farven er klar - der er ikke stivelse i.
Kammerjunker: Farven er sort - der er stivlese i.
Cocopops: Farven er sort - der er stivelse i.
Herefter opvarmer vi 50 ml vand til det koger. Når vandet så koger, tilsætter vi bundfaldet (stivelsen), og rører rundt. Så slukker vi for gassen, og holder bunden af det lille bægerglas (det med stivelsesblandingen) ned i et større glas med koldt vand. Her måler vi temperaturen, indtil den er faldet til 40 grader. Vi har nu fremstillet en stivelses-opløsning.
I næste forsøg fordeler vi en spytblandingen, der består af spyt og vand, i 4 reagensglas. Herefter tilsætter vi 1 dråbe stivelsesreagens i hvert glas. Så tilsætter vi 10 ml af stivelsesopløsningen i det første reagensglas. Derefter tilsætter vi 10 ml i det andet glas, så det tredje og til sidst det fjerde glas. Vi rører rundt i hvert glas efter tilsætningen.
Da alle fire glas har fået tilsat, hvad der skulle, sammenligner vi udseendet på væskerne. Alle væsker er blå, men vi kan se, at jo mere spyt, der er i glasset, jo lysere bliver farven. Det vil sige, at spyt nedbryder stivelsen.
Ved dette forsøg har vi også fundet ud af, at man kan dryppe nogle dråber stivelsesreagens på forskellige madvarer, og så kan man se, at jo mørkere madvaren bliver, jo mere stivelses er der i.
Forsøg 4: Påvisning er stivelse:
- faste stoffer drypper vi en dråbe stivelsesreagens på, for at se om der er stivelse i.
Abrikoser: Farven er klar - der er ikke stivelse i.
Kammerjunker: Farven er sort - der er stivlese i.
Cocopops: Farven er sort - der er stivelse i.
7.3 Protein i æg
Vi starter med at hælde 1/4 æggehvide i 2 reagensglas Herefter opvarmer vi det ene reagensglas i et vandbad (200 ml bægerglas med vand). Vi bliver ved med at varme æggehviden op, indtil den stivner. Da æggehvide er stivnet, er massen hvid og tyk. Så måler vi temperaturen på den stivnede æggehvide - den er 82,5 grader.
Forklaring på hvorfor vandbadet giver en langsom opvarmning af æggehviden:
Vandbadet giver en langsom opvarmning, da den først skal varme vandet op, og herefter æggehviden.
I næste forsøg hælder i den anden æggehvide i det (næsten) kogende vandbad, og rører derefter kraftigt rundt i massen. Massen er nu hvid, og har dannet en del skum på overfladen. Massen bliver også en smule grumset. Dette kaldes en opløsning af protein.
I det sidste forsøg tager vi 3 ml af den opløste proteinmasse og hælder det i et nyt reagensglas.Herefter hælder vi natriumhydroxid (NaOH) i reagensglaset, til rumfanget er fordoblet, hvorefter vi tilsætter 3-4 dråber kobbersulfat-opløsning og rører rundt. Nu er farven på massen lilla, hvilket er et bevis på, at der er proteiner i æggehviden.
Forsøg 4: Påvisning af proteiner i forskellige madvarer:
Abrikoser: Farven bliver kun gul, derfor er der ikke rigtig proteiner i. (2,9 g ca.)
Riskiks: Farven bliver kun lysebrun, derfor er der heller ikke ret mange proteiner i.
Bacon: Farve bliver lilla, derfor er der proteiner i. (ca 16 g.)
Forklaring på hvorfor vandbadet giver en langsom opvarmning af æggehviden:
Vandbadet giver en langsom opvarmning, da den først skal varme vandet op, og herefter æggehviden.
I næste forsøg hælder i den anden æggehvide i det (næsten) kogende vandbad, og rører derefter kraftigt rundt i massen. Massen er nu hvid, og har dannet en del skum på overfladen. Massen bliver også en smule grumset. Dette kaldes en opløsning af protein.
I det sidste forsøg tager vi 3 ml af den opløste proteinmasse og hælder det i et nyt reagensglas.Herefter hælder vi natriumhydroxid (NaOH) i reagensglaset, til rumfanget er fordoblet, hvorefter vi tilsætter 3-4 dråber kobbersulfat-opløsning og rører rundt. Nu er farven på massen lilla, hvilket er et bevis på, at der er proteiner i æggehviden.
Forsøg 4: Påvisning af proteiner i forskellige madvarer:
Abrikoser: Farven bliver kun gul, derfor er der ikke rigtig proteiner i. (2,9 g ca.)
Riskiks: Farven bliver kun lysebrun, derfor er der heller ikke ret mange proteiner i.
Bacon: Farve bliver lilla, derfor er der proteiner i. (ca 16 g.)
Fakta til 7.3:
Proteiner er opbygget i forlængelse af hinanden, og når der er mere end 100 aminosyrer i kæden, kaldes stoffet et protein.
-COOH = carbon, hydrogen, oxygen.
-NH2 = nitrogen og hydrogen
Proteiner er opbygget i forlængelse af hinanden, og når der er mere end 100 aminosyrer i kæden, kaldes stoffet et protein.
-COOH = carbon, hydrogen, oxygen.
-NH2 = nitrogen og hydrogen
7.4 Madolie og margarine
Vi starter med at dryppe en dråbe madolie på en stikke filtrerpapir. Ved siden af drypper vi en dråbe vand. Når dråberne er tørre, sammenligner vi dem. Vanddråben er bredt meget mere ud på papiret og er mere "gennemsigtig." Madoliedråben er mere tyk og fedtet, og den bredder sig heller ikke lige så meget ud. Hvis man lader papiret ligge, vil vanddråben også langsomt forsvinde, men det vil madolien ikke.
Herefter fylder vi 2 ml vand i et reagensglas, og hælder den dobbelte mængde madolie oveni. Madolien lægger sig her ovenpå vandet. Derefter sætter vi en prop i reagensglasset og ryster det kraftigt. Nu lader vi så glasset stå i et reagensglasstativ i nogle minutter. Vi kan nu konkludere, at madolien er lettere end vandet og derfor kan lægge sig ovenpå - og hermed flyde. Vi kan også se, at vand og olie ikke kan blandes.
I sidste forsøg tager vi en halv teske margarine og hælder i et reagensglas, hvorefter vi hælder 5 ml ethanol (sprit) ned til margarinen. Så sætter vi en prop i glasset og ryster det kraftigt. Det der sker i glasset er, at margarinen bliver mere glidende, og det klistrer sig ikke længere til glasset. Det skyldes, at ethanolen opløser fedtet.
Herefter hælder vi 5 ml vand i blandingen i reagensglasset og ryster det igen. Efter det har stået i nogle minutter, kan vi konkludere, at sprit og vand opløser margarinen, og hvis vi lader det stå i endnu længere tid, vil vi kunne se, at margarinen flyder opad.
Forsøg 3: Påvisning af fedt i forskellige madvarer:
Spegepølse: Dråben på papiret fordamper langsomt, derfor er der ikke så meget fedt i, men der er stadig en del.
Cocopops: Dråben på papiret fordamper langsomt, derfor er der ikke så meget fedt i.
Banan:
Herefter fylder vi 2 ml vand i et reagensglas, og hælder den dobbelte mængde madolie oveni. Madolien lægger sig her ovenpå vandet. Derefter sætter vi en prop i reagensglasset og ryster det kraftigt. Nu lader vi så glasset stå i et reagensglasstativ i nogle minutter. Vi kan nu konkludere, at madolien er lettere end vandet og derfor kan lægge sig ovenpå - og hermed flyde. Vi kan også se, at vand og olie ikke kan blandes.
I sidste forsøg tager vi en halv teske margarine og hælder i et reagensglas, hvorefter vi hælder 5 ml ethanol (sprit) ned til margarinen. Så sætter vi en prop i glasset og ryster det kraftigt. Det der sker i glasset er, at margarinen bliver mere glidende, og det klistrer sig ikke længere til glasset. Det skyldes, at ethanolen opløser fedtet.
Herefter hælder vi 5 ml vand i blandingen i reagensglasset og ryster det igen. Efter det har stået i nogle minutter, kan vi konkludere, at sprit og vand opløser margarinen, og hvis vi lader det stå i endnu længere tid, vil vi kunne se, at margarinen flyder opad.
Forsøg 3: Påvisning af fedt i forskellige madvarer:
Spegepølse: Dråben på papiret fordamper langsomt, derfor er der ikke så meget fedt i, men der er stadig en del.
Cocopops: Dråben på papiret fordamper langsomt, derfor er der ikke så meget fedt i.
Banan:
7.5 Vandindholdet i margarine
Vi starter med at finde 4 reagensglas. Det første glas fylder vi med flydende margarine, det andet med plantemargarine, det tredje med almindeligt margarine og det fjerde med smør. Herefter opvarmer vi et vandbad (500 ml bægerglas med vand) til 90 grader med alle 4 reagensglas i. Når vandbadet og glassene er helt oppe på 90 grader, tager vi glassene op og sammenligner dem. Man kan nu se, at olien (det gule) flyder ovenpå vandet. Der er mest olie i den flydende margarine, så den almindelige, så smøren, og det vil sige, at der er mindst olie i plantemargarinen.
Fra venstre: Almindeligt margarine, plantemargarine, smør og flydende.
Fra venstre: Almindeligt margarine, plantemargarine, smør og flydende.
7.6 Fremstilling af læskedrik
Opskrift på vores egen læskedrik:
I dette forsøg starter vi med at hælde 200 ml vand i et plastikglas. Herefter tilsætter vi 3 tsk sukker og en halv teske citronsyre. Vi kan nu smage på blandingen, at den er sød og lidt syrlig.
Derefter vil vi gerne have blandingen til at bruse, derfor tilsætter vi en teske natron - blandingen bruser.
(Man kan også tilsætte noget c-vitamin, hvis læskedrikken skal være sund)
Herefter tilsætter vi en halv teskefuld salt, så drikken bliver sund og isotonisk = mængdeforholdet mellem vand og salt i drikken skal være det samme som i kroppens blod og celler.
Opskrift på den bedste hjemmelavet læskedrik:
Vi hælder igen 200 ml vand i et plastikglas. Herefter tilsætter vi 1 spsk. og en halv teske sukker og en teskefuld citronsukker. Får at give drikken lidt mere smag tilsætter vi også meget lidt azorubin (jordbærsmag), så væsken også bliver rød. For at give brus tilsætter vi igen en smule natron. - Denne drik smager fantastisk!
I dette forsøg starter vi med at hælde 200 ml vand i et plastikglas. Herefter tilsætter vi 3 tsk sukker og en halv teske citronsyre. Vi kan nu smage på blandingen, at den er sød og lidt syrlig.
Derefter vil vi gerne have blandingen til at bruse, derfor tilsætter vi en teske natron - blandingen bruser.
(Man kan også tilsætte noget c-vitamin, hvis læskedrikken skal være sund)
Herefter tilsætter vi en halv teskefuld salt, så drikken bliver sund og isotonisk = mængdeforholdet mellem vand og salt i drikken skal være det samme som i kroppens blod og celler.
Opskrift på den bedste hjemmelavet læskedrik:
Vi hælder igen 200 ml vand i et plastikglas. Herefter tilsætter vi 1 spsk. og en halv teske sukker og en teskefuld citronsukker. Får at give drikken lidt mere smag tilsætter vi også meget lidt azorubin (jordbærsmag), så væsken også bliver rød. For at give brus tilsætter vi igen en smule natron. - Denne drik smager fantastisk!
7.7 Proteiner i mælk
I dette forsøg starter vi med at hælde 50 ml skummetmælk i et bægerglas. Herefter tilsætter vi 10 ml eddike og rører rundt med en spatel. Denne masse bliver hurtigt hvid og klumpet. Herefter tager vi et rent bægerglas og lægger et stykke gazebind henover. Nu skal vi så filtrere resten af mælken og eddiken fra i bægerglasset. De hvide klumper lægger sig på gazebindet, og det pakker vi derfor sammen, og presser i et tredje bægerglas med vand, så vi vallen og eddiken løber fra. Inde i gazebindet har vi nu begyndelsen til en ost.
De hvide klumper i stoffet består af store proteinmolekyler, der hedder kasein.
Resten af mælken, den tynde væske, kaldes valle.
I næste forsøg tager vi valle- og eddikevæsken og varmer op til 80 grader, så der bliver dannet en masse små hvide fnug. Herefter filtrere vi væsken med en trakt og et filtrerpapir ned i et nyt bægerglas.
De små hvide klumper i stoffet består af små proteinmolekyler, der hedder albumin. Resten af vallen indeholder mælkesukker.
De hvide klumper i stoffet består af store proteinmolekyler, der hedder kasein.
Resten af mælken, den tynde væske, kaldes valle.
I næste forsøg tager vi valle- og eddikevæsken og varmer op til 80 grader, så der bliver dannet en masse små hvide fnug. Herefter filtrere vi væsken med en trakt og et filtrerpapir ned i et nyt bægerglas.
De små hvide klumper i stoffet består af små proteinmolekyler, der hedder albumin. Resten af vallen indeholder mælkesukker.
7.8 Brusepulver
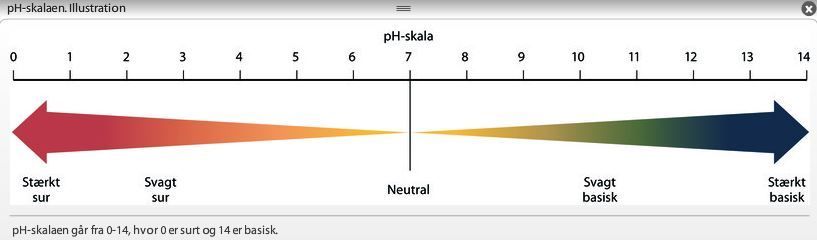
Vi starter med at blande en halv teske citronsyre med vand og måler derefter ph-værdien - denne blanding er sur. (Rød)
Herefter blander vi en halv teske natron med vand og måler igen ph-værdien - denne blanding er basis. (Blå)
Herefter tager vi 3 bægerglas med vand. I glas 1 tager vi og blander citronsyrer og natron, og det begynder at bruse.
I glas 2 blander vi citronsyre og sukker, og her sker ingenting. I glas 3 blander vi så natron og sukker, og her sker heller ingenting.
Herefter blander vi en teske citronsyre og en teske natron i et tørt bægerglas, for at se om de reagerer med hinanden. Her kan vi konkludere, at det gør de ikke. Herefter tilsætter vi 50 ml vand i glasset, hvor det begynder st bruse. Derefter skal vi prøve at stikke en brændende tændstik ned til blandingen, men ilden går med det samme ud, og røgen kan ikke komme op fra glasset. Dette sker fordi røgen er tungere end luft, og derfor kan det ikke komme op. Grunden til, at vi ikke kan stikke den brændende tændstik ned i glasset, er fordi, at vi har omdannet ilten i glasset til co2, og derfor "kvæler" pulverblandingen ilden.
Fakta til brusepulver:
Natriumhydrogencarbonat vil reagere som en base overfor citronsyre.
Reaktionen kan skrives: Natriumhydrogencarbonat + citronsyre = natriumcitrat + carbondioxid + vand.
Herefter blander vi en halv teske natron med vand og måler igen ph-værdien - denne blanding er basis. (Blå)
Herefter tager vi 3 bægerglas med vand. I glas 1 tager vi og blander citronsyrer og natron, og det begynder at bruse.
I glas 2 blander vi citronsyre og sukker, og her sker ingenting. I glas 3 blander vi så natron og sukker, og her sker heller ingenting.
Herefter blander vi en teske citronsyre og en teske natron i et tørt bægerglas, for at se om de reagerer med hinanden. Her kan vi konkludere, at det gør de ikke. Herefter tilsætter vi 50 ml vand i glasset, hvor det begynder st bruse. Derefter skal vi prøve at stikke en brændende tændstik ned til blandingen, men ilden går med det samme ud, og røgen kan ikke komme op fra glasset. Dette sker fordi røgen er tungere end luft, og derfor kan det ikke komme op. Grunden til, at vi ikke kan stikke den brændende tændstik ned i glasset, er fordi, at vi har omdannet ilten i glasset til co2, og derfor "kvæler" pulverblandingen ilden.
Fakta til brusepulver:
Natriumhydrogencarbonat vil reagere som en base overfor citronsyre.
Reaktionen kan skrives: Natriumhydrogencarbonat + citronsyre = natriumcitrat + carbondioxid + vand.
7.9 Fremstilling af alkohol
Vi starter med at fylde 4 reagensglas med vand. Herefter tilsætter vi en halv teskefuld druesukker i glas 1 og 3 og lukker åbningen med en ballon. I glas 2 og 4 tilsætter vi en halv teskefuld gær og lukker igen åbningen med en ballon. Glassene rystet til opløsning inden lukning. Vi lukker ikke glas 4 med en ballon, men opvarmer i stedet vandet til det koger.
Når væsken i glas 4 koger, tilsætter vi en halv teskefuld druesukker i blandingen, og lukker åbningen med en ballon.
Vi lader dette stå i nogle dage, så gæringen kan foregå.
Efter nogle dage er ballonen i glas 3 blevet pustet en smule op, da der er blevet dannet co2 ved hjælp af gæret. Det er derfor sukkeret og gæret, der danner processen.
Når væsken i glas 4 koger, tilsætter vi en halv teskefuld druesukker i blandingen, og lukker åbningen med en ballon.
Vi lader dette stå i nogle dage, så gæringen kan foregå.
Efter nogle dage er ballonen i glas 3 blevet pustet en smule op, da der er blevet dannet co2 ved hjælp af gæret. Det er derfor sukkeret og gæret, der danner processen.
7.10 Farvestoffer i krydderiet paprika
Vi starter med at hælde 20 ml vand i et 100 ml bægerglas. Herefter tilsætter vi en halv teske paprika og 10 dråber sprit. Så rører vi rundt i blandingen. Derefter tager vi et langt stykke kridt og sætter i midten af glasset. For at kridtet bliver i midten af glasset og blandingen sætter vi tape på. Nu venter vi til at væsken er steget næsten til toppen af kridtet.
Da kridtet ikke virker helt så godt, sætter vi også et kromatografipapir ned i væsken, og ser efter når farven stiger op af papiret.
Vi kan i dette forsøg se, at der ikke er brugt Sudan Rød, som er ulovligt, da der ikke kommer nogen farve. Der er derfor ikke tilsat farvestoffer.
Da kridtet ikke virker helt så godt, sætter vi også et kromatografipapir ned i væsken, og ser efter når farven stiger op af papiret.
Vi kan i dette forsøg se, at der ikke er brugt Sudan Rød, som er ulovligt, da der ikke kommer nogen farve. Der er derfor ikke tilsat farvestoffer.
7.11 Farvestoffer i slik
I dette forsøg starter vi med at hælde 50 ml vand i et 100 ml bægerglas. Herefter putter vi 5 lilla smarties ned i vandet og rører rundt, til farven fra chokoladen er opløst i vandet (Vandet bliver blå/lilla). Herefter sætter vi et stykke filtrerpapir i en tragt og placerer tragten i en kolbe. Nu filtrerer vi halvdelen af vandet ned i kolben.
Imens tager vi endnu en kolbe, tragt og filtrerpapir og hælder resten af vandet i. Dette vand filtrerer vi så sammen med noget aktivt kul. Vi kan nu sammenligne de to forskellige filtreret vandtyper. Vi kan konkludere, at det aktive kulstof trækker farven ud af vandet, da farven nærmest bliver gennemsigtigt i stedet for farvet.
Imens tager vi endnu en kolbe, tragt og filtrerpapir og hælder resten af vandet i. Dette vand filtrerer vi så sammen med noget aktivt kul. Vi kan nu sammenligne de to forskellige filtreret vandtyper. Vi kan konkludere, at det aktive kulstof trækker farven ud af vandet, da farven nærmest bliver gennemsigtigt i stedet for farvet.
7-10-7.11 Farvestoffer i smarties
Vi starter dette forsøg på samme måde som i forsøg 7.11, ved at hælde 50 ml vand i et lille bægerglas. Derefter putter vi 3 lyserøde smarties ned i vandet og rører rundt, indtil farven er rørt helt ud af chokoladen (vandet er nu lilla/blå.) Herefter filtrerer vi alt vandet ned i en kolbe, ved hjælp af en tragt og filtrerpapir. Så drypper vi 10 dråber sprit ned i det filtrerede vand, hvorefter vi rører rundt. Derefter sætter vi et stykke kromatografipapir ned i vandet og lader det stå et stykke tid, for at se hvilke farvestoffer der er blevet brugt i smartiesne.
7.13 Gæring (1)
Vi starter med at blande 10g sukker og 10g gær i en 250 ml. kolbe. Derefter opvarmer vi et halvt fyldt bægerglas (stort) til den valgte temperatur, som er 30 grader. Når vandet har temperaturen, hælder vi 100 ml. af vandet over i kolben.
Herefter laver vi en gærlås: Vi sætter en prop med et glasrør fast i kolben, og sætter en gummislange fast fra glasrøret og ned i et reagensglas, der er 2/3 fyld med vand.
Så sætter vi kolben ned i det opvarmede vand, og nu skal vi så se, om vandet i reagensglasset begynder at boble pga. gæring. Vi kan nu konkludere, at ved en opvarming på kun 30 grader, skal vi ryste kolben, for at det begynder at boble. Temperaturen skal derfor være højere, hvis gæret skal være mere aktivt og dermed boble mere.
Herefter laver vi en gærlås: Vi sætter en prop med et glasrør fast i kolben, og sætter en gummislange fast fra glasrøret og ned i et reagensglas, der er 2/3 fyld med vand.
Så sætter vi kolben ned i det opvarmede vand, og nu skal vi så se, om vandet i reagensglasset begynder at boble pga. gæring. Vi kan nu konkludere, at ved en opvarming på kun 30 grader, skal vi ryste kolben, for at det begynder at boble. Temperaturen skal derfor være højere, hvis gæret skal være mere aktivt og dermed boble mere.
7.13 Gæring (2)
Vi starter med at opløse 1g gær i 10 ml lunkent vand, herefter blander vi det sammen i en skål med 20g hvedemel, 10 ml vand og 0,5g salt.
Teori til madens kemi
- Mineraler = grundstoffer.
- Kulhydrater og fedt er energikilder - gør at vi kan fungere.
- Kulhydrater, fedtstoffer og proteiner, mineraler, vitaminer og vand er kroppens byggesten.
- proteiner består af aminosyrer, og de opbygger cellerne. (Hvis man sætter aminosyrer sammen, danner man et protein)
- Der er 20 forskellige aminosyrer til at danne proteinerne.
- Disse aminosyrer kaldes essentielle (livsnødvendige)
- kulhydrat - kul = carbon, hydrat = vand - carbonvand fx. mest simple sukkerform glukose. (se formel øverst ^)
- Den mest simple form for sukker er monosacchariderne (se igen formlen øverst)
- to monosaccharider + vand = dissacharider
- C6H12O6 + C6H12=6 --> C12H22O11 + H2O
- Polysaccharider, de største molekyler af sukker. De er opbygget som en kæde af monosaccharider. Forstavelsen "poly" betyder mange. Stivelse og cellulose er polysaccharider. Et stivelsesmolekyle indeholder 200 til 2000 glucosemolekyler.
- Der er stivelse i mange fødevarer, fx brød, kartofler og ris. Ren stivelse er et hvidt pulver uden lugt og smag. Fibrene i planter og træ er opbygget af cellulose. Det er ekstra lange polysaccharider.
- Glucose = druesukker
- Tomater indeholder fructose
- Et voksent menneske skal hver dag spise 60g proteiner.
- Børn skal have flere proteiner end voksne, da de skal vokse.
- proteiner = kød, bønner, ost og æg fx.
- Proteiner er også betegnet som æggehvidestoffer.
- Der findes 50000 proteiner i kroppen.
Fedtstoffer:
- I kroppe har fedtet fire vigtige opgaver:
1. Fedt skal give energi til kroppen.
2. Fedt skal bringe de fedtopløselige vitaminer A, D, E og K ud til kroppens celler
3. Fedt skal isolere kroppen, så der ikke afgives for meget varme til omgivelserne.
4. fedt skal virke atødabsorberende for kroppens indre organer.
- fedt kan oplagres i kroppen, indtil det skal bruges af cellerne for at producere energi.
- Alle fedtstoffer er opbygget på samme måde. Molekylerne består oftest af tre fedtsyrer, der holdes fast af stoffet glycetol. De forskellige fedtstoffer indeholder forskellige fedtsyrer. En meget kendt fedtsyre er stearinsyre.
- Alle organiske syrer slutter på COOH
Mættede fedtsyrer:
- En mættet fedtsyre (SFA) er en fedtsyre, der ikke indeholder nogle dobbeltbindinger mellem de enkelte kulstof-atomer. Jo flere mættede fedtsyrer, der er i et fedtstof, jo mere fast er fedtstoffet.
- Mættede fedtsyrer findes hovedsageligt i animalsk fedt, herunder også mælkefedt (smør, ost med mere).
- Mættede fedtsyrer er de usunde fedtsyrer.
Umættede fedtsyrer:
- Umættede fedtsyrer indeholder dobbeltbindinger mellem kulstof-atomerne.
- Mono-umættede fedtsyrer indeholder én dobbeltbinding, og poly-umættede fedtsyrer indeholder to eller flere dobbeltbindinger.
- Jo mere umættet et fedtstof er, jo mere flydende er det.
- Umættede fedtsyrer er de "sunde" fedtsyrer.
- Umættede fedtsyrer inddeles i familier afhængig af placeringen af den sidste dobbeltbinding i molekylet. Det er hovedsageligt tre fedtsyrerfamilier, der har interesse. Nemlig omega-3-fedtsyrer, omega-6-fedtsyrer og omega-9-fedtsyrer.
Eksempler på umættede fedtsyrer (sunde):
- Avokade, fede fisk (laks, ørred, ål og makrel), kerne (solsikkekerne og pinjekerner), Olier (rapsolie, olivenolie, vindruekerneolie), Nødder (peanuts, hasselnødder, pistacienødder, valnødder)
Eksempler på mættede fedtsyrer (usunde):
- Chips (flæskesvær og franske kartofler), Pommes frites, chokolade, kager(wienerbrød), fede mejeriprodukter (ost, sødmælk, flødeis), smør, fedt kød (spegepølse, rullepølse, kødpølse), bacon.
Fedt og vand kan ikke lide hinanden, derfor lægger olie sig også ovenpå vandet, hvis man blander det.
- Olie er upolært, vand er polært.
- Polært kan blandes med andre polære stoffer.
- Fedt kan ikke lede strøm, men det kan vand.
- Polært = Har en positiv og negativ ladning og kan lede strøm.
- Kulhydrater og fedt er energikilder - gør at vi kan fungere.
- Kulhydrater, fedtstoffer og proteiner, mineraler, vitaminer og vand er kroppens byggesten.
- proteiner består af aminosyrer, og de opbygger cellerne. (Hvis man sætter aminosyrer sammen, danner man et protein)
- Der er 20 forskellige aminosyrer til at danne proteinerne.
- Disse aminosyrer kaldes essentielle (livsnødvendige)
- kulhydrat - kul = carbon, hydrat = vand - carbonvand fx. mest simple sukkerform glukose. (se formel øverst ^)
- Den mest simple form for sukker er monosacchariderne (se igen formlen øverst)
- to monosaccharider + vand = dissacharider
- C6H12O6 + C6H12=6 --> C12H22O11 + H2O
- Polysaccharider, de største molekyler af sukker. De er opbygget som en kæde af monosaccharider. Forstavelsen "poly" betyder mange. Stivelse og cellulose er polysaccharider. Et stivelsesmolekyle indeholder 200 til 2000 glucosemolekyler.
- Der er stivelse i mange fødevarer, fx brød, kartofler og ris. Ren stivelse er et hvidt pulver uden lugt og smag. Fibrene i planter og træ er opbygget af cellulose. Det er ekstra lange polysaccharider.
- Glucose = druesukker
- Tomater indeholder fructose
- Et voksent menneske skal hver dag spise 60g proteiner.
- Børn skal have flere proteiner end voksne, da de skal vokse.
- proteiner = kød, bønner, ost og æg fx.
- Proteiner er også betegnet som æggehvidestoffer.
- Der findes 50000 proteiner i kroppen.
Fedtstoffer:
- I kroppe har fedtet fire vigtige opgaver:
1. Fedt skal give energi til kroppen.
2. Fedt skal bringe de fedtopløselige vitaminer A, D, E og K ud til kroppens celler
3. Fedt skal isolere kroppen, så der ikke afgives for meget varme til omgivelserne.
4. fedt skal virke atødabsorberende for kroppens indre organer.
- fedt kan oplagres i kroppen, indtil det skal bruges af cellerne for at producere energi.
- Alle fedtstoffer er opbygget på samme måde. Molekylerne består oftest af tre fedtsyrer, der holdes fast af stoffet glycetol. De forskellige fedtstoffer indeholder forskellige fedtsyrer. En meget kendt fedtsyre er stearinsyre.
- Alle organiske syrer slutter på COOH
Mættede fedtsyrer:
- En mættet fedtsyre (SFA) er en fedtsyre, der ikke indeholder nogle dobbeltbindinger mellem de enkelte kulstof-atomer. Jo flere mættede fedtsyrer, der er i et fedtstof, jo mere fast er fedtstoffet.
- Mættede fedtsyrer findes hovedsageligt i animalsk fedt, herunder også mælkefedt (smør, ost med mere).
- Mættede fedtsyrer er de usunde fedtsyrer.
Umættede fedtsyrer:
- Umættede fedtsyrer indeholder dobbeltbindinger mellem kulstof-atomerne.
- Mono-umættede fedtsyrer indeholder én dobbeltbinding, og poly-umættede fedtsyrer indeholder to eller flere dobbeltbindinger.
- Jo mere umættet et fedtstof er, jo mere flydende er det.
- Umættede fedtsyrer er de "sunde" fedtsyrer.
- Umættede fedtsyrer inddeles i familier afhængig af placeringen af den sidste dobbeltbinding i molekylet. Det er hovedsageligt tre fedtsyrerfamilier, der har interesse. Nemlig omega-3-fedtsyrer, omega-6-fedtsyrer og omega-9-fedtsyrer.
Eksempler på umættede fedtsyrer (sunde):
- Avokade, fede fisk (laks, ørred, ål og makrel), kerne (solsikkekerne og pinjekerner), Olier (rapsolie, olivenolie, vindruekerneolie), Nødder (peanuts, hasselnødder, pistacienødder, valnødder)
Eksempler på mættede fedtsyrer (usunde):
- Chips (flæskesvær og franske kartofler), Pommes frites, chokolade, kager(wienerbrød), fede mejeriprodukter (ost, sødmælk, flødeis), smør, fedt kød (spegepølse, rullepølse, kødpølse), bacon.
Fedt og vand kan ikke lide hinanden, derfor lægger olie sig også ovenpå vandet, hvis man blander det.
- Olie er upolært, vand er polært.
- Polært kan blandes med andre polære stoffer.
- Fedt kan ikke lede strøm, men det kan vand.
- Polært = Har en positiv og negativ ladning og kan lede strøm.
Drikkevarer
Kroppen skal have vand for at erstatte det vand, der forsvinder med udåndingsluften og med sveden.
Når sveden på kroppen fordamper, afkøles kroppen. Sammenlign med
Når sveden på kroppen fordamper, afkøles kroppen. Sammenlign med
Sportsdrik
En sportsdrik skal give kroppen tre ting: vand, salte og energi.
Kroppen skal have tilført de salte, som tabes med sveden, og kroppe skal have energi i form af sukker (kulhydrat.)
Det sendes rundt i kroppen med blodet. Sukkeret i blodet kaldes blodsukker. Mængden af sukker i blodet skal holdes på en fast koncentration. Falder blodsukkeret under en vis koncentration, går man "sukkerkold," og præsentationsevnen falder.
Den perfekte sportsdrik:
En sportsdrik skal indeholde salte svarende til sammensætningen af normal sved. Sportsdrikken kan indeholde flere forskellige former for sukker. Det mest almindelige er at benytte glukose (druesukker.) Det er den sukkerform, som findes i blodet, og som hurtigst optages i kroppen. I en isotonisk sportsdrik er mængdeforholdet mellem vand og salt det samme som i kroppens celler og i blodet. Mængden af sukker ligger fra 6 til 8%.
Kroppen skal have tilført de salte, som tabes med sveden, og kroppe skal have energi i form af sukker (kulhydrat.)
Det sendes rundt i kroppen med blodet. Sukkeret i blodet kaldes blodsukker. Mængden af sukker i blodet skal holdes på en fast koncentration. Falder blodsukkeret under en vis koncentration, går man "sukkerkold," og præsentationsevnen falder.
Den perfekte sportsdrik:
En sportsdrik skal indeholde salte svarende til sammensætningen af normal sved. Sportsdrikken kan indeholde flere forskellige former for sukker. Det mest almindelige er at benytte glukose (druesukker.) Det er den sukkerform, som findes i blodet, og som hurtigst optages i kroppen. I en isotonisk sportsdrik er mængdeforholdet mellem vand og salt det samme som i kroppens celler og i blodet. Mængden af sukker ligger fra 6 til 8%.
Mælk
Mælk fra en ko indeholder næsten 90% vand og ofte fra 3 til 4% fedt. Fedt er ikke opløseligt i vand. I mælk flyder en mængde små fedtkugler rundt i vandet. Størrelsen af fedtkugler er mindre end 1/50 mm. Fedtkuglerne klumper ikke sammen, fordi de er omgivet af proteiner og membran. En sådan fedtkugle omgivet af en membran kaldes en micelle. Fedtmicellerne gør mælken uigennemsigtig og giver mælken dens hvidgule farve. Hvis fedtkuglerne fjernes, bliver mælken blålig, som fx. skummetmælk. I mælk findes også calcium-ioner, Ca2+, og forskellige phosphat-ioner. De er alle vigtige for at få sunde knogler og tænder.
På mejeriet
Når mælken kommer til mejeriet, bliver den centrifugeret. Da fedtkuglerne vejer mindre end resten af mælken, samler fedtkuglerne sig i midten af centrifugen som fløde. Den fjernes, og af noget af den fremstilles smør.
Undercentrifugeringen opvarmes mælken i kort tid til 75 grader, så bakterier slås ihjel. Mælken er nu pasteuriseret.
Mælken kan herefter blive homogeniseret. Ved denne proces omdannes store fedtkugler til minde. De mindre kugler kan lettere flyde rundt i mælken uden at klumpe sig sammen og uden at stige op til et lag fløde.
Undercentrifugeringen opvarmes mælken i kort tid til 75 grader, så bakterier slås ihjel. Mælken er nu pasteuriseret.
Mælken kan herefter blive homogeniseret. Ved denne proces omdannes store fedtkugler til minde. De mindre kugler kan lettere flyde rundt i mælken uden at klumpe sig sammen og uden at stige op til et lag fløde.
Vand med brus
Mange drikkevarer indeholder carbondioxid, CO2. Det giver en syrlig smag. Når man åbner for en sådan flaske, dannes en masse små bobler af CO2, der stiger til vejrs. Det giver en "prikkende" smag,
Mineralvand og sodavand får CO2 tilsat kunstigt. CO2 pumpes ved højt tryk ned i væsken, hvor størstedelen af CO2 opløses i vandet.
H2O + CO2 = H2CO3
Vin, øl og champagne:
I vin og champagne opstår CO2-indholdet ved gæring. Sukkeret i druesaften omdannes af gærceller til akohol og CO2.
Reaktionen skrives: C8H12O6 --> 2 C2H5OH + 2 CO2
Alkoholen, C2H5OH, har det kemiske navn ethanol, der i daglig tale kaldes sprit.
Det er den samme reaktion, der sker ved fremstilling af øl. Her er det sukkeret i kornsorten byg, der omdannes til ethanol og CO2. Under gæringen slipper der CO1 ud til omgivelserne. Derfor har man i bryggerier en grænseværdi for, hvor højt indholdet af carbondioxid i luften må blive. Her regner man med en grænseværdi på 0,5%.
Når man laver champagne, tilsætter man ekstra sukker, så der dannes meget CO2. Herved bliver trykket i flasken meget højt. Det kan være farligt. I en ølflaske er trykket ikke så højt.
Mineralvand og sodavand får CO2 tilsat kunstigt. CO2 pumpes ved højt tryk ned i væsken, hvor størstedelen af CO2 opløses i vandet.
H2O + CO2 = H2CO3
Vin, øl og champagne:
I vin og champagne opstår CO2-indholdet ved gæring. Sukkeret i druesaften omdannes af gærceller til akohol og CO2.
Reaktionen skrives: C8H12O6 --> 2 C2H5OH + 2 CO2
Alkoholen, C2H5OH, har det kemiske navn ethanol, der i daglig tale kaldes sprit.
Det er den samme reaktion, der sker ved fremstilling af øl. Her er det sukkeret i kornsorten byg, der omdannes til ethanol og CO2. Under gæringen slipper der CO1 ud til omgivelserne. Derfor har man i bryggerier en grænseværdi for, hvor højt indholdet af carbondioxid i luften må blive. Her regner man med en grænseværdi på 0,5%.
Når man laver champagne, tilsætter man ekstra sukker, så der dannes meget CO2. Herved bliver trykket i flasken meget højt. Det kan være farligt. I en ølflaske er trykket ikke så højt.