1.1 Atomet og dets kerne
1: Atomkerne er positivt ladet.
2: Elektroner er negativt ladet.
3: Kernen i hydrogen består af en proton.
4: Joseph John Thomson opdagede elektronen.
5: Ernest Rutherford opdagede atomkernen.
6: 0,4 nm er 0,0000004 mm. (0,4 * 10^-7)
7: Der kan ligge 2500000 jern-atomer på en række med længden 1 mm. (1/0,0000004)
2: Elektroner er negativt ladet.
3: Kernen i hydrogen består af en proton.
4: Joseph John Thomson opdagede elektronen.
5: Ernest Rutherford opdagede atomkernen.
6: 0,4 nm er 0,0000004 mm. (0,4 * 10^-7)
7: Der kan ligge 2500000 jern-atomer på en række med længden 1 mm. (1/0,0000004)
1.2 Flammefarver (1)
Først skal vi finde ud af den kraftigste farve natrium udsender, og det er en meget kraftig gul, der ligger mellem 500 og 600.
Det første stof vi tog, var calciumchlorid. Vi puttede 1/3 vand i et reagensglas og fugtede glassets spids. Derefter stak vi spidsen ind i toppen af bunsenbrænderflammen, og flammen blev kraftig orange-rød. Derefter kiggede vi på flammen igennem et håndspektometer, og der kom 3 farver - grøn, orange og rød.
Derefter skiftede vi stoffet ud med natriumchlorid, og gjorde nøjagtigt det samme som før. Flammen uden håndspektometeret var meget kraftig orange, men med håndspektometeret var farverne de samme som før - grøn, orange og rød.
Det første stof vi tog, var calciumchlorid. Vi puttede 1/3 vand i et reagensglas og fugtede glassets spids. Derefter stak vi spidsen ind i toppen af bunsenbrænderflammen, og flammen blev kraftig orange-rød. Derefter kiggede vi på flammen igennem et håndspektometer, og der kom 3 farver - grøn, orange og rød.
Derefter skiftede vi stoffet ud med natriumchlorid, og gjorde nøjagtigt det samme som før. Flammen uden håndspektometeret var meget kraftig orange, men med håndspektometeret var farverne de samme som før - grøn, orange og rød.
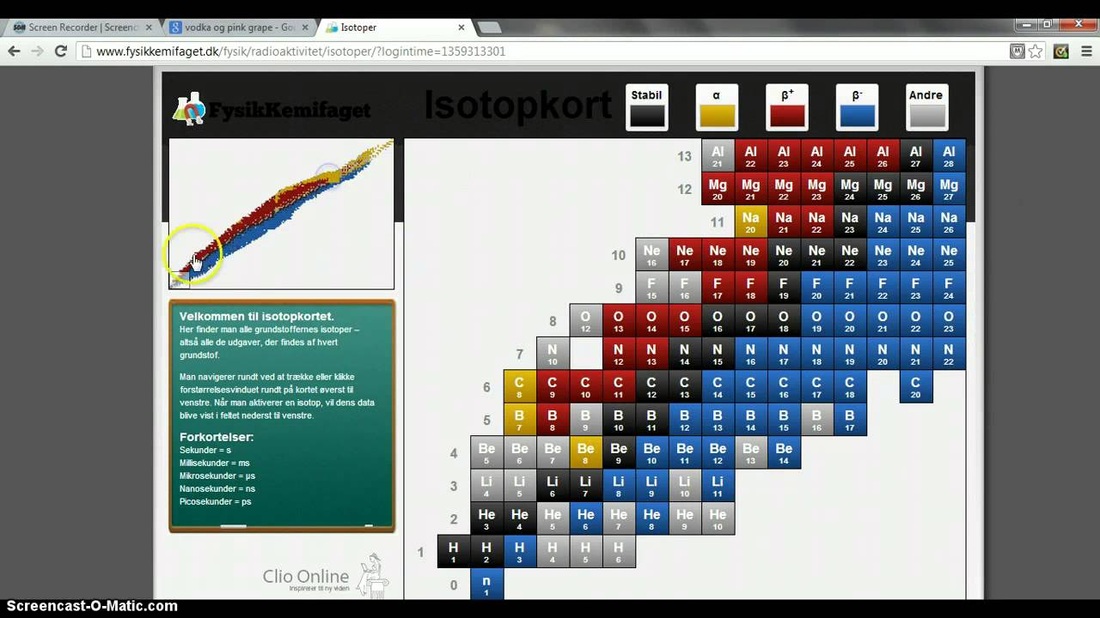
Isotopkort - hvordan virker det?
Dette er et udvidet periodisk system, også kaldt et isotopkort.
I dette system er alle typerne af et grundstof samlet. Som man kan se er alle heliumstofferne samlet på en række, fordi der findes forskellige slags af det samme grundstof. Tallet under bogstaverne viser, hvor mange atomer der er i kernen.
Her er et eksempel: 6 He = 6 atomer i kernen, 2 protoner. Tallet 6 hedder nukleontallet, og tallet 2 er atomnummeret/grundstofnummeret.
Man finder ud af hvor mange elektroner, der er i grundstoffet, ved at minus nukleontallet og atomnummeret.
I dette system er alle typerne af et grundstof samlet. Som man kan se er alle heliumstofferne samlet på en række, fordi der findes forskellige slags af det samme grundstof. Tallet under bogstaverne viser, hvor mange atomer der er i kernen.
Her er et eksempel: 6 He = 6 atomer i kernen, 2 protoner. Tallet 6 hedder nukleontallet, og tallet 2 er atomnummeret/grundstofnummeret.
Man finder ud af hvor mange elektroner, der er i grundstoffet, ved at minus nukleontallet og atomnummeret.
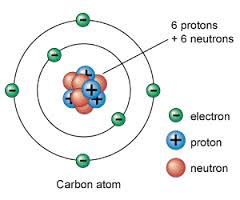
Atomets opbygning:
Dette er atomet Carbon. Man kan se det er grundstof nr. 6, da det har 6 protoner i atomkernen.
Indhold + udseende:
Man ved at der inde i kernen er protoner, som er positivt ladet, og der er neutroner, som er neutrale. Atomkernen er meget lille i forhold til selve atomet, som er omringet af elektroner, son er negativt ladet.
Elektronerne befinder sig ud i skaller rundt om kernen.
Et atom indeholder lige så mange protoner og elektroner - det vil sige at det er elektrisk ladet.
Både en proton og neutron vejer 1 unit, mens en elektron vejer 1/2000 unit. Det vil sige at der skal 2000 elketroner til, før den vejer lige så meget som en proton.
Elektronerne befinder sig ud i skaller rundt om kernen.
Et atom indeholder lige så mange protoner og elektroner - det vil sige at det er elektrisk ladet.
Både en proton og neutron vejer 1 unit, mens en elektron vejer 1/2000 unit. Det vil sige at der skal 2000 elketroner til, før den vejer lige så meget som en proton.
Tidslinje:
I gamle dage: Her forestillede man sig at det var en lille kugle, som ikke kunne deles i mindre dele.
For 2400 år siden: Demokrit mente, at hvis man blev ved med at halvere et stof, ville det til sidst blive så lille at intet kunne blive/være mindre.
1897: Elektronen blev opdaget.
Slutningen af 1800 og starten af 1900: Der blev lavet en masse forsøg, og de forsøg har gjort udfaldet til det vi ved i dag.
1911: Ernest Rutherford opdagede i 1911 at atomet havde en meget lille kerne.
1913: Niels Bohr finder ud af, at det er elektronerne der udsender lys, når vi fx har et stearinlys tændt.
For 2400 år siden: Demokrit mente, at hvis man blev ved med at halvere et stof, ville det til sidst blive så lille at intet kunne blive/være mindre.
1897: Elektronen blev opdaget.
Slutningen af 1800 og starten af 1900: Der blev lavet en masse forsøg, og de forsøg har gjort udfaldet til det vi ved i dag.
1911: Ernest Rutherford opdagede i 1911 at atomet havde en meget lille kerne.
1913: Niels Bohr finder ud af, at det er elektronerne der udsender lys, når vi fx har et stearinlys tændt.
Atomer og det periodiske system
Protonerne og neutronerne sidder inde i kernen, og elektronerne sidder ude på skallen. Elektrontallet kan varierer, men det kan protontallet ikke - derfor kan man se på antallet af protoner, hvilket grundstof det er.
6 He = 6 atomer i kernen, 2 protoner. Tallet 6 hedder nukleontallet, og tallet 2 er
atomnummeret/grundstofnummeret
Man finder ud af hvor mange elektroner, der er i grundstoffet, ved at minus nukleontallet og atomnummeret.
Antallet af protoner i et bestemt grundstofs atomkerne er det samme som stoffets nummer i det periodiske system.
En enhed der forkortes skrives med u. Både protoner og neutroner har en masse tæt ved 1 u. Elektronens masse er meget mindre, bare 0,0005 u. Det er 1/2000 af protonens masse.
Isotoper, i et bestemt grundstofs kerne kan der være forskelligt antal neutroner. Atomer med samme antal protoner, men med et forskelligt antal neutroner, kaldes isotoper.
Isotoper er altså et grundstof med forskellige masser.
I kemiske processer er der ingen forskel på de to isotoper. Når de reagerer med oxygen, dannes vand H2O. I almindeligt vand indeholder 99,985% af molekylerne den lette hydrogen isotop. Men vand indeholder ganske lidt, 0,015% tungt vand ed isotopen deutrium.
Massen af 1 ml almindeligt vand er præcis 1 gram, men samme mængde tungt vand med to deuterium-isotoper i molekylet har massen 1,11 g.
6 He = 6 atomer i kernen, 2 protoner. Tallet 6 hedder nukleontallet, og tallet 2 er
atomnummeret/grundstofnummeret
Man finder ud af hvor mange elektroner, der er i grundstoffet, ved at minus nukleontallet og atomnummeret.
Antallet af protoner i et bestemt grundstofs atomkerne er det samme som stoffets nummer i det periodiske system.
En enhed der forkortes skrives med u. Både protoner og neutroner har en masse tæt ved 1 u. Elektronens masse er meget mindre, bare 0,0005 u. Det er 1/2000 af protonens masse.
Isotoper, i et bestemt grundstofs kerne kan der være forskelligt antal neutroner. Atomer med samme antal protoner, men med et forskelligt antal neutroner, kaldes isotoper.
Isotoper er altså et grundstof med forskellige masser.
I kemiske processer er der ingen forskel på de to isotoper. Når de reagerer med oxygen, dannes vand H2O. I almindeligt vand indeholder 99,985% af molekylerne den lette hydrogen isotop. Men vand indeholder ganske lidt, 0,015% tungt vand ed isotopen deutrium.
Massen af 1 ml almindeligt vand er præcis 1 gram, men samme mængde tungt vand med to deuterium-isotoper i molekylet har massen 1,11 g.
Kopiside 1.3
Kopiark 1.3:
Hvor mange protoner er der i et carbon-atom?
Der er 6 protoner i et carbon-atom.
Hvad hedder grundstoffet med nr. 8, og hvor mange protone indeholder det?
Grundstof nr. 8 hedder oxygen, og det har 8 protoner.
Hvor mange nukleoner er der i sølv-atomets kerne?
Der er 107 nukleoner i sølv-atomets kerne.
Hvor mange protoner og neutroner er der i sølv-atomets kerne?
Der er 47 protoner og 60 neutroner.
Formlen for et natrium-atom og hvor mange neutroner er der i kernen?
Formlen er 23 NA, det vil sige at der er 11 neutroner i kernen.
11
Hvilket atom indeholder flest protoner, af et guld- elle sølv-atom?
Det gør et guld-atom, den har 79 protoner og et sølv-atom har 47 protoner i kernen.
Hvad er tungt vand?
Tungt vand er vand, der har fået erstattet en eller begge brintatomer H med den tungere, stabile isotop ²H – eller D (for deuterium). F.eks. DHO eller D2O.
Deuterium består populært sagt af én neutron, én proton og én elektron. Dermed er deuterium tungere end 1H = H, da deuterium har en neutron mere.
Tung is, lavet af frossent tungt vand D2O, har en massefylde på 1,108 g/cm3 og vil derfor synke i almindeligt vand.
Skema:
Hvor mange protoner er der i et carbon-atom?
Der er 6 protoner i et carbon-atom.
Hvad hedder grundstoffet med nr. 8, og hvor mange protone indeholder det?
Grundstof nr. 8 hedder oxygen, og det har 8 protoner.
Hvor mange nukleoner er der i sølv-atomets kerne?
Der er 107 nukleoner i sølv-atomets kerne.
Hvor mange protoner og neutroner er der i sølv-atomets kerne?
Der er 47 protoner og 60 neutroner.
Formlen for et natrium-atom og hvor mange neutroner er der i kernen?
Formlen er 23 NA, det vil sige at der er 11 neutroner i kernen.
11
Hvilket atom indeholder flest protoner, af et guld- elle sølv-atom?
Det gør et guld-atom, den har 79 protoner og et sølv-atom har 47 protoner i kernen.
Hvad er tungt vand?
Tungt vand er vand, der har fået erstattet en eller begge brintatomer H med den tungere, stabile isotop ²H – eller D (for deuterium). F.eks. DHO eller D2O.
Deuterium består populært sagt af én neutron, én proton og én elektron. Dermed er deuterium tungere end 1H = H, da deuterium har en neutron mere.
Tung is, lavet af frossent tungt vand D2O, har en massefylde på 1,108 g/cm3 og vil derfor synke i almindeligt vand.
Skema:
Kopiside 1.4
Internetsider vi bruger:
Ordbogen.com
Google oversæt
www.ptable.com
Nucleus Win
Grundstof på engelsk?
Element
Det periodiske system på engelsk?
The periodic table
Det engelske navn for...?
Bly: Lead
Kalium: Potassium
Kviksølv: Mercury/quicksilver
Jern: Iron
Kobber: Copper
Natrium: Sodium
Hvad hedder silicon og sulfur på dansk?
Silicon: Silicium
Sulfur: Svovl
Hvad hedder hydrogen og oxygen på svensk?
Hydrogen: Väte
Oxygen: Syre
Atom navn, protoner, neutroner, nukleoner i 48,22 Ti:
Atomnavnet er Titan.
Der er 22 protoner.
Der er 26 neutroner
Der er 48 nukleoner.
Formlen for almindeligt og tungt hydrogen:
Almindeligt hydrogen: 1,1 H
Tungt hydrogen: 2, 1 H
Neutroner som hver jern-isotop har, når de har 54, 56 og 57 nukleoner:
54: Den har 28 neutroner.
56: Den har 30 neutroner.
57: Den har 31 neutroner.
Hvor mange stabile isotoper findes der af guld, standardformlen:
Der er en stabil isotop.
197, 79 AU.
Hvilket stof har ni stabile isotoper?
Det er grundstoffet Xenon der har ni isotoper. Det er grundstof nr. 54.
Oxygen har 3 stabile isotoper. Hvilken isotop er der mest af?
Den første, er den almindelige, med 8 protoner og 8 neutroner.
Dena anden har 8 protoner og 9 neutroner.
Den sidste har 8 protoner og 10 neutroner.
Forstår ikke det med mest af?
Hvor mange procent udgør uran-235 af almindelig uran?
Kan ikke finde ud af. (?)
5 grundstoffer der kun har 1 stabil isotop, på de første 3 rækker:
Den første er beryllium, så Fluorine, Sodium/Natrium, Aluminium og Phosphorus/Fosfor
Hvor mange protoner er der i sølv-atomets kerne?
Der er 47 protoner.
Hvad er navnet og nummeret på Hg, Nb og P?
Nb = Niobium, nummer 41.
P = Fosfor, nummer 15.
Hg = Kviksølv, nummer 80.
Hvilke grundstof har flest stabile isotoper?
Tin har flest stabile isotoper - nemlig 10.
Hvilke grundstof med et nummer under 82 har ikke stabile isotoper?
Grundstof nummer 43, Technetium - Tc (??)
Ordbogen.com
Google oversæt
www.ptable.com
Nucleus Win
Grundstof på engelsk?
Element
Det periodiske system på engelsk?
The periodic table
Det engelske navn for...?
Bly: Lead
Kalium: Potassium
Kviksølv: Mercury/quicksilver
Jern: Iron
Kobber: Copper
Natrium: Sodium
Hvad hedder silicon og sulfur på dansk?
Silicon: Silicium
Sulfur: Svovl
Hvad hedder hydrogen og oxygen på svensk?
Hydrogen: Väte
Oxygen: Syre
Atom navn, protoner, neutroner, nukleoner i 48,22 Ti:
Atomnavnet er Titan.
Der er 22 protoner.
Der er 26 neutroner
Der er 48 nukleoner.
Formlen for almindeligt og tungt hydrogen:
Almindeligt hydrogen: 1,1 H
Tungt hydrogen: 2, 1 H
Neutroner som hver jern-isotop har, når de har 54, 56 og 57 nukleoner:
54: Den har 28 neutroner.
56: Den har 30 neutroner.
57: Den har 31 neutroner.
Hvor mange stabile isotoper findes der af guld, standardformlen:
Der er en stabil isotop.
197, 79 AU.
Hvilket stof har ni stabile isotoper?
Det er grundstoffet Xenon der har ni isotoper. Det er grundstof nr. 54.
Oxygen har 3 stabile isotoper. Hvilken isotop er der mest af?
Den første, er den almindelige, med 8 protoner og 8 neutroner.
Dena anden har 8 protoner og 9 neutroner.
Den sidste har 8 protoner og 10 neutroner.
Forstår ikke det med mest af?
Hvor mange procent udgør uran-235 af almindelig uran?
Kan ikke finde ud af. (?)
5 grundstoffer der kun har 1 stabil isotop, på de første 3 rækker:
Den første er beryllium, så Fluorine, Sodium/Natrium, Aluminium og Phosphorus/Fosfor
Hvor mange protoner er der i sølv-atomets kerne?
Der er 47 protoner.
Hvad er navnet og nummeret på Hg, Nb og P?
Nb = Niobium, nummer 41.
P = Fosfor, nummer 15.
Hg = Kviksølv, nummer 80.
Hvilke grundstof har flest stabile isotoper?
Tin har flest stabile isotoper - nemlig 10.
Hvilke grundstof med et nummer under 82 har ikke stabile isotoper?
Grundstof nummer 43, Technetium - Tc (??)
1.9 Svækkelse af stråling:
Hvilken slags ioniserende stråling udsender kilden?
Vi har valgt gammastråling og de 2 andre.
Hvad, hvorfor, hverdag...
HVAD:
Vi skal finde ud af intensiteten på strålingen alt efter hvor lang afstanden er. Vi starter med en afstand mellem geigerrøret og gammakilden på 27 cm. Derefter måler vi strålingen, som viser at målingen er på 9,8 i gennemsnittet.
Derefter laver vi en afstand på 22 cm og måler igen: Gennemsnittet er denne gang på 13,8.
Igen rykker vi gammakilden tættere på, så afstanden nu er 17 cm. Gennemsnittet er nu steget til 21,2. Sådan bliver vi ved med at rykke gammakilden 5 cm. tættere på, indtil sidst hvor vi rykker den 2 cm.
Afstand på 12 cm: Gennemsnittet = 31,5.
Afstand på 7 cm: Gennemsnittet = 78,6.
Afstand på 5 cm: Gennemsnit = 135,2.
Afstand på 3 cm: Gennemsnit = 286,7.
Afstand på 1 cm: Gennemsnit = 933,8.
Derefter tager vi en betastråling:
Her starter vi også med en afstand mellem betastrålingen og geigercounteren på 27 cm. Vi foretager forsøget på helt samme måde som med gammastrålingen.
Afstand på 25 cm: Gennemsnit = 17,83
Afstand på 20 cm: Gennemsnit = 25,83.
Afstand på 15 cm: Gennemsnit = 44.
Afstand på 10 cm: Gennemsnit = 87,33.
Afstand på 5 cm: Gennemsnit = 230,16.
Afstand på 3 cm: Gennemsnit = 522,5.
Afstand på 1 cm: Gennemsnit = 1328,83.
Til sidst tager vi alfastrålingen:
Vi foretager herefter alfastrålingen på nøjagtigt den samme måde.
Afstand på 25 cm: Gennemsnit = 4,33.
Afstand på 20 cm: Gennemsnit = 4,67.
Afstand på 15 cm: Gennemsnit = 3,5
Afstand på 10 cm: Gennemsnit = 3,8
Afstand på 5 cm: Gennemsnit = 9,33
Afstand på 3 cm: Gennemsnit = 16,6.
Afstand på 1 cm: Gennemsnit = 101,17.
Afstand på 2 mm: Gennemsnit = 2560,67.
HUSK:
Gamma er mere gennemtrængende, da det er en bølgestråling, hvorimod beta og alfa er partikelstråling.
Hvad kan strålingerne trænge igennem/Hvad er forskellen?:
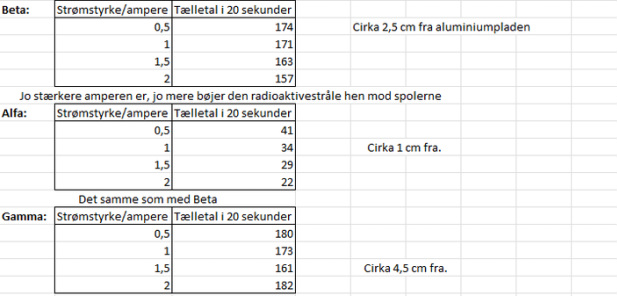
Først sammenligner vi vores resultater med alfa. Vi starter derfor med at holde et stykke karton mellem alfastrålen og geigercounteren. Uden kartonet i mellem var gennemsnittet på 1 cm i afstand 101,17, men med kartonet foran er gennemsnittet kun 40,5. Det vil derfor sige, at alfa er meget svag og knap nok kan trænge igennem et enkelt stykke karton. Derefter holder vi 3 stykker karton ind foran, men det gør ikke rigtig nogen forskel, da gennemsnittet stadig kun er på 40,16. Der er derfor også en forskel på 61. Alfastrålingen kan stadig ikke trænge igennem kartonstykkerne, om så der er 1 eller 3 stykker foran.
Herefter sammenligner vi resultaterne på gamma. Vi starter denne gang med at holde et stykke bly ind foran. Gennemsnittet var 933,8 uden blyet, og med blyet er gennemsnittet 347. Der er derfor en forskel på 586. Det vil derfor sige, at gamma ikke er helt så stærk og gennemtrængende, når det kommer til bly.
Til sidst tager vi betastrålingen. Her holder vi en aluminiumsplade ind foran. Resultatet uden pladen var fra før 1328,83, hvilket viser at beta er meget kraftig. Efter forsøget med aluminiumspladen, har vi fundet ud af at gennemsnittet er på 93,3, derfor er der en forskel på 1235. Det vil derfor sige, at aluminiumspladen er meget kraftig, og derfor kan betastrålen ikke trænge igennem, men beta ville derimod sagtens kunne trænge igennem kartonet, da det er en meget kraftig stråling.
Herefter prøver vi med 2 aluminiumsplader, og her er gennemsnittet helt nede på 5,5, hvilket også bare viser, at det er en kraftig metode.
Herefter prøver vi, hvor godt de 3 forskellige strålinger kan trænge igennem en glasplade:
Vi prøver først med betastrålingen. Her er gennemsnittet 25, hvilket viser, at glaspladen er så kraftig, at selv ikke beta kan trænge nemt igennem.
Bagefter prøver vi med gammastrålingen, som har et gennemsnit på 305,83, hvilket beviser, at gamma kan trænge igennem stort set alt. Glaspladen er stadig meget kraftig, men gamma er så gennemtrængende, at den nemt kan trænge igennem.
Til sidst prøver vi med alfastrålingen, som har et gennemsnit på 26,16, hvilket viser, at selvom alfa er meget svag, kan det godt trænge igennem en glasplade.
HVORFOR - konklusion:
Vi finder ud af at der er forskel på alfa, beta og gamma. Man kan ikke konkludere stålingen ud af en kilde. Gamma er mere kraftig og gennemtrængende. Udover det kan vi konkludere at alfa er meget svag og kan ikke engang trænge igennem luften. Vi kan også se, at beta er meget mere gennemtrængende end både alfa og gamma. Det vil også sige, at alfa ikke er farlig, men at man skal være meget opmærksom på betastråling.
HVERDAG:
Man kan bruge dette i hverdagen da man kan finde ud af hvor kraftig og om man skal passe på strålingen. Alfa er ikke så farlig, men gamma der i mod er meget gennemtrængende, og den skal man tage mere afstand til.
Når vi bruger capstone?
Når vi bruger capstone til radioaktivitet, skal vi huske, at man for det meste skal bruge "geiger müller counter," og i stedet for 20 herz, skal vi vælge 10.00 s, så den måler strålingen hvert 10 sekund.
Alfa: En heliumkerne = positivt ladet. Den vejer 4 Unit. Den har en kort rækkevidde i luft - 1-2 cm. Papir kan stoppe Alfa - meget stor.
Beta: En elektron = negativt ladet. Den vejer 1/2000 Unit. Lang rækkevidde i luft - 8-10 cm. Aluminium kan stoppe Beta.
Gamma: EMB = Elektromagnetiskebølge. Mellem rækkevidde i luft - 6-7 cm. Bly og 1-2 m beton kan stoppe Gamma.
Vi har valgt gammastråling og de 2 andre.
Hvad, hvorfor, hverdag...
HVAD:
Vi skal finde ud af intensiteten på strålingen alt efter hvor lang afstanden er. Vi starter med en afstand mellem geigerrøret og gammakilden på 27 cm. Derefter måler vi strålingen, som viser at målingen er på 9,8 i gennemsnittet.
Derefter laver vi en afstand på 22 cm og måler igen: Gennemsnittet er denne gang på 13,8.
Igen rykker vi gammakilden tættere på, så afstanden nu er 17 cm. Gennemsnittet er nu steget til 21,2. Sådan bliver vi ved med at rykke gammakilden 5 cm. tættere på, indtil sidst hvor vi rykker den 2 cm.
Afstand på 12 cm: Gennemsnittet = 31,5.
Afstand på 7 cm: Gennemsnittet = 78,6.
Afstand på 5 cm: Gennemsnit = 135,2.
Afstand på 3 cm: Gennemsnit = 286,7.
Afstand på 1 cm: Gennemsnit = 933,8.
Derefter tager vi en betastråling:
Her starter vi også med en afstand mellem betastrålingen og geigercounteren på 27 cm. Vi foretager forsøget på helt samme måde som med gammastrålingen.
Afstand på 25 cm: Gennemsnit = 17,83
Afstand på 20 cm: Gennemsnit = 25,83.
Afstand på 15 cm: Gennemsnit = 44.
Afstand på 10 cm: Gennemsnit = 87,33.
Afstand på 5 cm: Gennemsnit = 230,16.
Afstand på 3 cm: Gennemsnit = 522,5.
Afstand på 1 cm: Gennemsnit = 1328,83.
Til sidst tager vi alfastrålingen:
Vi foretager herefter alfastrålingen på nøjagtigt den samme måde.
Afstand på 25 cm: Gennemsnit = 4,33.
Afstand på 20 cm: Gennemsnit = 4,67.
Afstand på 15 cm: Gennemsnit = 3,5
Afstand på 10 cm: Gennemsnit = 3,8
Afstand på 5 cm: Gennemsnit = 9,33
Afstand på 3 cm: Gennemsnit = 16,6.
Afstand på 1 cm: Gennemsnit = 101,17.
Afstand på 2 mm: Gennemsnit = 2560,67.
HUSK:
Gamma er mere gennemtrængende, da det er en bølgestråling, hvorimod beta og alfa er partikelstråling.
Hvad kan strålingerne trænge igennem/Hvad er forskellen?:
Først sammenligner vi vores resultater med alfa. Vi starter derfor med at holde et stykke karton mellem alfastrålen og geigercounteren. Uden kartonet i mellem var gennemsnittet på 1 cm i afstand 101,17, men med kartonet foran er gennemsnittet kun 40,5. Det vil derfor sige, at alfa er meget svag og knap nok kan trænge igennem et enkelt stykke karton. Derefter holder vi 3 stykker karton ind foran, men det gør ikke rigtig nogen forskel, da gennemsnittet stadig kun er på 40,16. Der er derfor også en forskel på 61. Alfastrålingen kan stadig ikke trænge igennem kartonstykkerne, om så der er 1 eller 3 stykker foran.
Herefter sammenligner vi resultaterne på gamma. Vi starter denne gang med at holde et stykke bly ind foran. Gennemsnittet var 933,8 uden blyet, og med blyet er gennemsnittet 347. Der er derfor en forskel på 586. Det vil derfor sige, at gamma ikke er helt så stærk og gennemtrængende, når det kommer til bly.
Til sidst tager vi betastrålingen. Her holder vi en aluminiumsplade ind foran. Resultatet uden pladen var fra før 1328,83, hvilket viser at beta er meget kraftig. Efter forsøget med aluminiumspladen, har vi fundet ud af at gennemsnittet er på 93,3, derfor er der en forskel på 1235. Det vil derfor sige, at aluminiumspladen er meget kraftig, og derfor kan betastrålen ikke trænge igennem, men beta ville derimod sagtens kunne trænge igennem kartonet, da det er en meget kraftig stråling.
Herefter prøver vi med 2 aluminiumsplader, og her er gennemsnittet helt nede på 5,5, hvilket også bare viser, at det er en kraftig metode.
Herefter prøver vi, hvor godt de 3 forskellige strålinger kan trænge igennem en glasplade:
Vi prøver først med betastrålingen. Her er gennemsnittet 25, hvilket viser, at glaspladen er så kraftig, at selv ikke beta kan trænge nemt igennem.
Bagefter prøver vi med gammastrålingen, som har et gennemsnit på 305,83, hvilket beviser, at gamma kan trænge igennem stort set alt. Glaspladen er stadig meget kraftig, men gamma er så gennemtrængende, at den nemt kan trænge igennem.
Til sidst prøver vi med alfastrålingen, som har et gennemsnit på 26,16, hvilket viser, at selvom alfa er meget svag, kan det godt trænge igennem en glasplade.
HVORFOR - konklusion:
Vi finder ud af at der er forskel på alfa, beta og gamma. Man kan ikke konkludere stålingen ud af en kilde. Gamma er mere kraftig og gennemtrængende. Udover det kan vi konkludere at alfa er meget svag og kan ikke engang trænge igennem luften. Vi kan også se, at beta er meget mere gennemtrængende end både alfa og gamma. Det vil også sige, at alfa ikke er farlig, men at man skal være meget opmærksom på betastråling.
HVERDAG:
Man kan bruge dette i hverdagen da man kan finde ud af hvor kraftig og om man skal passe på strålingen. Alfa er ikke så farlig, men gamma der i mod er meget gennemtrængende, og den skal man tage mere afstand til.
Når vi bruger capstone?
Når vi bruger capstone til radioaktivitet, skal vi huske, at man for det meste skal bruge "geiger müller counter," og i stedet for 20 herz, skal vi vælge 10.00 s, så den måler strålingen hvert 10 sekund.
Alfa: En heliumkerne = positivt ladet. Den vejer 4 Unit. Den har en kort rækkevidde i luft - 1-2 cm. Papir kan stoppe Alfa - meget stor.
Beta: En elektron = negativt ladet. Den vejer 1/2000 Unit. Lang rækkevidde i luft - 8-10 cm. Aluminium kan stoppe Beta.
Gamma: EMB = Elektromagnetiskebølge. Mellem rækkevidde i luft - 6-7 cm. Bly og 1-2 m beton kan stoppe Gamma.
Kopiside 1.8
To magneter - Beta tiltrækkes af plus, og Alfa tiltrækkes af minus, Gamma går lige igennem.
kopiside 1.10 - styring med betastråling
Vi starter med at fylde et halv reagensglas med vand, hvorefter vi sætter det fast i et stativ. Derefter tilslutter vi et geigermüllerrør til capstone på computeren. Vi begynder så at kører geigermüllerrøret på den ene side af reagensglasset, og på den anden side kører vi betapartiklen. Vi skal nu finde ud af, om vandet kan svække strålingen, og det kan den. Vi kan høre på klikkene fra geigerrøret, at vandet svækker en hel del, og det kan også aflæses ud fra capstone, da tælleren bliver højere, når der ikke er vand imellem.
Vi startede med at veje massen af reagensglasset og vandet. Det vejede 47g.
Bagefter ruller vi papir omkring reagensglasset, og hælder vand i glasset med en sprøjteflaske, indtil tælletallet på capstone begynder at falde. Herefter vejer vi igen massen, og den er denne gang på 43g. Formålet med at vikle reagensglasset ind i papir, er at vi skulle prøve at kunne høre på klikkene fra geigerrøret, hvor meget vand vi havde hældt i. Vi skal derfor se, om vi kunne ramme stregen ved halvdelen af reagensglasset.
Herefter gentager vi forsøget for igen at prøve, om vi kan ramme halvdelen af glasset med vand ved at lytte til klikkene fra geigerrøret. Denne gang vejer massen herefter kun 40g, det vil derfor sige, at vi ikke helt kunne høre på klikkene, hvornår glasset var halvt fyldt.
Ud fra vores beregninger kan vi se, at vores første forsøg var 4g fra den samlede vægt af vandets masse, og vores andet forsøg var 7g fra den samlede vægt af vandets masse.
Ud fra dette forsøg har vi fundet ud af, at hvis man lavede en lille sprække eller noget lignende, som strålingen kunne ramme igennem, ville man kunne få et mere præcis sted, hvor strålingen ville ramme, da strålingen udsender stråler i alle mulige tilfældige retninger, som den er nu.
Man kan ud fra dette, finde ud af hvor meget væske der er - røgalarm.
Vi startede med at veje massen af reagensglasset og vandet. Det vejede 47g.
Bagefter ruller vi papir omkring reagensglasset, og hælder vand i glasset med en sprøjteflaske, indtil tælletallet på capstone begynder at falde. Herefter vejer vi igen massen, og den er denne gang på 43g. Formålet med at vikle reagensglasset ind i papir, er at vi skulle prøve at kunne høre på klikkene fra geigerrøret, hvor meget vand vi havde hældt i. Vi skal derfor se, om vi kunne ramme stregen ved halvdelen af reagensglasset.
Herefter gentager vi forsøget for igen at prøve, om vi kan ramme halvdelen af glasset med vand ved at lytte til klikkene fra geigerrøret. Denne gang vejer massen herefter kun 40g, det vil derfor sige, at vi ikke helt kunne høre på klikkene, hvornår glasset var halvt fyldt.
Ud fra vores beregninger kan vi se, at vores første forsøg var 4g fra den samlede vægt af vandets masse, og vores andet forsøg var 7g fra den samlede vægt af vandets masse.
Ud fra dette forsøg har vi fundet ud af, at hvis man lavede en lille sprække eller noget lignende, som strålingen kunne ramme igennem, ville man kunne få et mere præcis sted, hvor strålingen ville ramme, da strålingen udsender stråler i alle mulige tilfældige retninger, som den er nu.
Man kan ud fra dette, finde ud af hvor meget væske der er - røgalarm.
kOpiside 1.11 - baggrundsstråling
Vi starter med at tilslutte et geigermüllerrør til en geigermüllercounter, og så måler vi baggrundsstrålingen i 5 minutter. Tælletallet er herefter 11. Derfor er tælletallet pr minut 2,2 på baggrundsstråling.
Herefter vil vi måle det radioaktive stof i NaCl (fint salt) i et minut, og derefter skal vi huske at trække baggrundsstrålingen fra. Vi putter derfor først lidt fint køkkensalt i et lille bægerglas og dækker det med et papir. Herefter måler vi radioaktiviteten i 1 minut. Tælletallet var på 8, det vil sige at vi trækker 2,2 fra 8, og det giver 5,8. Derfor er tælletallet på radioaktivt stof i NaCl på 5,8.
Derefter gentager vi forsøget med calciumklorid, hvor tælletallet også når op på 8. Igen trækker vi baggrundsstrålingen fra, og derfor er tælletallet på radioaktivt stof igen 5,8.
Udfra dette forsøg kan vi konkludere, at der er en radioaktiv isotop i disse stoffer, da deres tælletal er højere end baggrundsstrålingen.
Kan komme fra støv, lidt fra mennesker, byggematerialer, undergrunden, rummet, maden vi spiser.
Herefter vil vi måle det radioaktive stof i NaCl (fint salt) i et minut, og derefter skal vi huske at trække baggrundsstrålingen fra. Vi putter derfor først lidt fint køkkensalt i et lille bægerglas og dækker det med et papir. Herefter måler vi radioaktiviteten i 1 minut. Tælletallet var på 8, det vil sige at vi trækker 2,2 fra 8, og det giver 5,8. Derfor er tælletallet på radioaktivt stof i NaCl på 5,8.
Derefter gentager vi forsøget med calciumklorid, hvor tælletallet også når op på 8. Igen trækker vi baggrundsstrålingen fra, og derfor er tælletallet på radioaktivt stof igen 5,8.
Udfra dette forsøg kan vi konkludere, at der er en radioaktiv isotop i disse stoffer, da deres tælletal er højere end baggrundsstrålingen.
Kan komme fra støv, lidt fra mennesker, byggematerialer, undergrunden, rummet, maden vi spiser.
kopiark 1.7 - halveringstid af Cs-137 (1)
Vi starter med at sætte et geigermüllerrør til capstone på computeren. Derefter tager vi noget saltvand i en sprøjte, og sætter sprøjten fast på en cs-137 kerne, hvor der sidder en gummislange i den anden ende. Så sprøjter vi lidt af saltvandet ned på en plastikplade, og rykker det ind foran geigerrøret. Fordi saltvandet har været igennem cs-137 kernen, bliver saltvandet med det samme radioaktivt. Derefter måler vi strålingen i 8 minutter.
Så måler vi halveringstiden på det højeste tælletal, som er 873. Udfra grafen i capstone kan vi aflæse, at 873 bliver halveret til 436 på 2 minutter og 20 sekunder, derfor er der en halveringstid på 2 minutter og 20 sekunder på saltvandets stråling.
Man skal selvfølgelig altid huske at trække baggrundsstrålingen fra, så en måling på 873, er faktisk kun på 870,8.
Derefter skal vi finde ud af hvor på grafen, at halveringstiden er mest nøjagtigt, og det har vi fundet frem til, at den er på starten af grafen, fordi
Så måler vi halveringstiden på det højeste tælletal, som er 873. Udfra grafen i capstone kan vi aflæse, at 873 bliver halveret til 436 på 2 minutter og 20 sekunder, derfor er der en halveringstid på 2 minutter og 20 sekunder på saltvandets stråling.
Man skal selvfølgelig altid huske at trække baggrundsstrålingen fra, så en måling på 873, er faktisk kun på 870,8.
Derefter skal vi finde ud af hvor på grafen, at halveringstiden er mest nøjagtigt, og det har vi fundet frem til, at den er på starten af grafen, fordi